
近年来,非瘟疫苗在全球范围内获得显著突破,我们今天就来讲一讲疫苗到底研究到了哪一步。
一、灭活苗
在非洲猪瘟疫苗的研究历史中,灭活苗是最早被开发出来的,不同实验证实灭活苗的保护率只有0%-70%。
可分为病毒灭活和病毒致弱灭活;
不能对强毒攻击提供有效的免疫保护;
可产生高效价的抗体,很难检测到中和抗体;
新型佐剂 Polygen 或 Emulsigen-D的应用:可产生ASFV特异性抗体,但未能提高疫苗的免疫保护效力;
细胞免疫在ASF灭活疫苗免疫保护中起重要作用;
低代次和高代次的ASFV毒株对中和抗体的敏感性存在差异。
二、减毒活疫苗
可以诱导强烈持久的免疫应答,与其他类型疫苗相比,弱毒苗的保护性更高,但生物安全是其使用的主要限制因素。
目前可通过基因重组、靶向缺失以及一次性侵染技术来增强减毒活疫苗的安全性。
弱毒苗主要分为自然弱毒苗、传代弱毒苗和重组弱毒苗。
1、自然弱毒苗
自然弱毒苗是从自然界中分离到的非洲猪瘟弱毒株,如天然致弱毒株OURT88/3或NH/P68;
自然弱毒苗可以产生对同源强毒株的攻毒保护,依据实验动物和攻毒毒株的不同,保护率介于66%-100%;
OURT88/3毒株产生的免疫保护与病毒特异性IFN-γ产生细胞呈正相关;
交叉保护疫苗: OURT88/3免疫并用致病性OURT88/1毒株进行加强免疫,产生针对 ASFV-I型不同分离毒株的保护;
这类疫苗在强毒攻毒的实验中得到的保护率很高,很多可以达到100%,但是副作用和安全性问题突出。副反应: 发热、关节肿胀、肺炎、流产、死亡等,慢性感染;
其中研究比较多,比较有前景的是Lv17/WB/Rie1毒株。
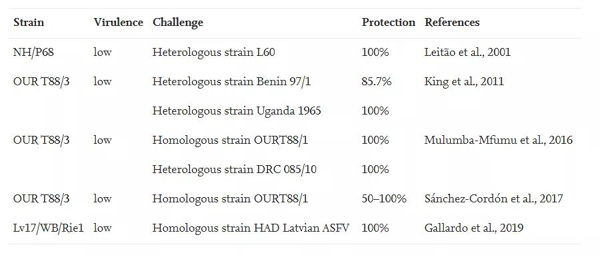
图1 已公开的自然弱毒苗
2、传代弱毒苗
强毒株经过猪骨髓来源细胞、Vero和COS-1等敏感细胞系进行的传代致弱。
ASFV致病力逐渐下降,但病毒免疫原性和稳定性也随之下降;
1960年代,西班牙和葡萄牙使用传代致弱毒株免疫动物用于非瘟净化,但是产生了灾难性的后果, 呈现出肺炎、流产和死亡等副作用;
田间多次感染和异源强毒株存在的条件下,免疫动物呈现ASF慢性感染。
3、重组弱毒苗
一般通过敲除病毒功能基因、毒力基因、免疫抑制基因来设计疫苗;
降低病毒毒力或增加机体对病毒的免疫应答;
比传统弱毒疫苗安全性更好, 效力更高的基因工程减毒活疫苗;
目前研究设计的毒力基因包括TK(K196R)、9GL(B119L)、CD2v(EP402R)、DP148R、 NL(DP71L)、UK(DP96R)和多基因家族360,505(MGF360/505)
缺失毒株接种宿主毒力减弱, 产生针对同源毒株或异源毒株的免疫保护
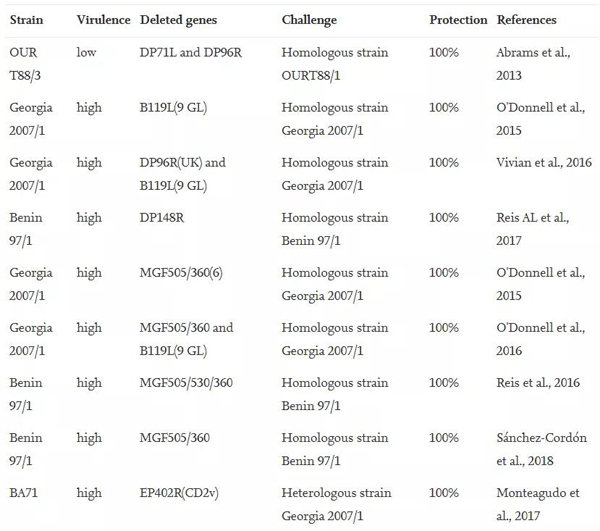
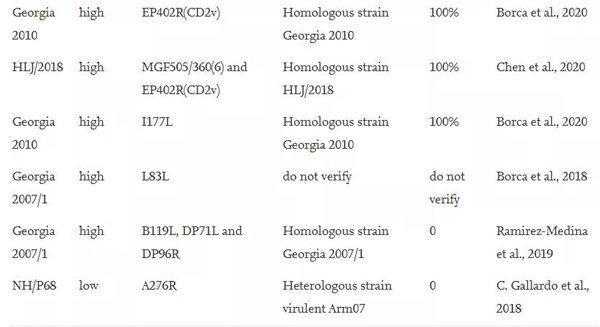
图2 已公开的重组弱毒苗
三、活载体疫苗
通常使用腺病毒或痘病毒作为载体:可引起细胞免疫和CTL反应;
“鸡尾酒”式免疫:
人腺病毒Ad5载体+ ①ASFV-p32、p54、p72和pp62;或②ASFV-A151R、B119L、B602L、EP402RΔPRR、B438L和K205R-A104R;
可引起良好的抗原特异性CTL反应,以及强烈的体液免疫反应和细胞免疫应答。
四、核酸疫苗
将编码病毒主要抗原的基因克隆入真核表达载体后直接导入机体内,在宿主细胞内完成转录翻译后产生抗原蛋白,从而同时激活体液免疫和细胞免疫应答。
ASFV DNA疫苗(p72、p30和p54):不能够提供攻毒保护;
ASFV DNA疫苗(p30、p54、猪白细胞抗原II):无ASFV抗体,部分动物获得攻毒保护;
ASFV DNA疫苗(表达文库):60%的保护力,有待于发掘更多保护性抗原;
五、亚单位疫苗
杆状病毒表达系统:p72、p30和p54等,不能提供有效的免疫攻毒保护,说明仅仅依靠上述抗原刺激产生的中和抗体很难 获得理想的免疫保护效果。
人源293(HEK)细胞表达系统:B646L(p72)、E183L(p54)和O61R(p12),与痘病毒载体疫苗进行首免-加强免疫,获得较好的体液免疫和细胞免疫水平。
六、展望
对于减毒活疫苗来说,无论是采用经典方法还是通过基因操作,它们都能提供较好的保护水平,(至少对同源毒株是如此)。这一战略被认为更接近市场,几乎所有的研究小组都寄希望于此。
最新发布