
一、猪轮状病毒(RV)
1975年以来,RV被认为是导致猪只腹泻的主要原因之一。RV易感所有日龄的猪只,对哺乳和断奶仔猪影响最大。RV可能导致一个猪群的大范围流行性腹泻,导致新生仔猪的严重发病率和死亡率,造成猪场严重的经济损失。因为RV的多样性,而且RV导致猪只发病的机制还需进一步的研究,RV对猪场养殖成本的影响还需进一步的计算。
美国农业部每隔6-8年做一次生猪的调查。2000年、2006年和2012年的调查结果显示,猪生产者怀疑RV是导致猪只发病死亡的比率分别为5.7%、6.9%和19.4%,呈上升趋势。

二、猪的RV流行率
目前,已知有五种不同的RV感染猪,包括RVA、RVB、RVC、RVE和RVH。RVA是世界各地发现的最常见的猪感染和引起腹泻的RV类型(Molinari等人,2016)。RVA是1975年在猪身上发现和分离的第一个RV物种(Rodger等人,1975年;Woode等人,1976年)。目前,猪RVA G基因型至少有12种,包括G1、G2、G3、G4、G5、G6、G8、G9、G10、G11、G12和G26;猪RVA P基因型至少有13种,包括P[1]、P[5]、P[6]、P[7]、P[8]、P[11]、P[13]、P[19]、P[23]、P[26]、P[27]、P[32]和P[34](Naseer等人,2017)。其中,猪中最常见的G基因型包括G3、G4、G5、G9和G11,最常见的两种P基因型包括:P[6]和P[7](Lorenzetti等人,2011)。
20世纪80年代首次在猪中发现一种非典型的RV,被命名为RVB。在日本、德国、美国、加拿大、墨西哥和印度的猪中都有RVB的报道。RVB在粪便中的排毒量低,偶尔发生感染情况。
1980年,在俄亥俄州的一头27天大的仔猪身上首次发现了RVC(Saif等人,1980年)。RVC有可能诱发亚临床感染或引起猪只腹泻的大规模暴发(Marthaler等人,2014a)。在美国、巴西、加拿大和整个欧洲的猪群中检测到了RVC(Chepngeno等人,2019年)。它通常会感染1至20日龄的仔猪(Chepngeno等人,2020年;Marthaler等人,2014a)。目前,已知有7种RVC G基因型(包括G1、G3、G5、G6、G7、G8和G9)和6种P基因型(包括P[1]、P[2]、P[3]、P[4]、P[5]和P[6])感染猪(Theuns等人,2016)。两种最常见的RVC G基因型是G3和G6(Vlasova等人,2017)。
迄今为止,RVE只在英国一个猪只临床样品中检测到。其临床重要性和其多样性等还未知。
1991-1995年间,一种新的RV在日本引起30日龄以下仔猪腹泻(Suzuki&Inoue,2018)。直到1999年,才在MA104细胞中鉴定并分离出一种新的猪种RVH,即毒株SKA-1(Wakuda et al.,2011)。Marthaler等人(2014b)从2006年至2009年间采集的204份样本中调查了美国猪群中是否存RVH。十个州的样品中30%呈阳性。在美国,RVH通常在21-55日龄和55日龄或以上的猪只中检测到。据推测,可能与美国猪只的断奶实践相关。同样,2012年,Molinari等人(2014年)在巴西35日龄仔猪的三个粪便样本中检测到RVH。
三、传播
母猪通常是RV的亚临床携带者,并将粪便中的RV感染性病毒颗粒排放到环境中。仔猪感染通常发生在断奶前直接接触母猪或断奶后接触其它猪只通过粪口方式感染。这些感染也可通过受污染的食物、水和寄生虫间接发生(Chandler Bostock&Mellits,2015)。
四、发病机理
RV的发病机制始于病毒开始在位于小肠绒毛顶端的成熟肠细胞(上皮细胞)的细胞质中复制。随着RV感染的进展,“小肠上皮组织出现广泛的细胞坏死,导致绒毛萎缩,消化酶丧失,吸收减少,肠腔渗透压增加,并出现腹泻”(Desselberger等人,2009)。
五、临床症状
在猪中,RV感染的严重程度取决于宿主和病毒因素。猪群体中RV毒株的毒力可能受到病毒株、病毒感染剂量、宿主年龄、受影响的消化细胞数量、宿主免疫状态、宿主环境、营养以及宿主是否同时存在其它感染的影响(Dewey等人,2003;Kahn&Line,2005;威尔等人,1994年)。通过RT-qPCR,研究人员发现每一种RV都倾向于感染不同的年龄组。这将在第3章中详细讨论。当RV感染的临床症状出现时,包括脱水、厌食、生长抑制和轻度至重度腹泻(Saif&Fernandez,1996)。轮状病毒可感染所有年龄的猪,但通常感染新生仔猪(<7日龄)和断奶仔猪(21至28日龄)。新生仔猪的临床症状包括出生后12-48小时的水样腹泻,当新生仔猪没有从母猪获得足够的保护性母源抗体时,或在断奶后母源抗体趋于下降时发生。在哺乳仔猪(5至21日龄)中,腹泻通常呈黄色或灰色,两天后变为灰色和糊状。在感染期间,哺乳仔猪的腹泻可以持续两到五天。断奶仔猪通常会出现水样腹泻,其中含有消化不良的饲料(Kahn&Line,2005)。
六、病变
RV感染的严重损害通常在1至14日龄的仔猪中更为严重。胃通常充满食物,小肠壁薄、松弛,并伴有水样液体扩张(Chang et al.,2012;Kahn&Line,2005)。消化道、盲肠和结肠含有更多的液体粪便。大体病变在21天及以上变为轻度至无。
实验感染RVA的无菌猪提供了更好的研究方式。口服RV后15~18小时,小肠绒毛顶端上皮细胞开始退化。在16-24小时内,绒毛萎缩发生的细胞脱落和感染24-72小时后严重程度增加。在48-72小时内,记录到隐窝上皮增生(Chang等人,2012年)。图1a-c分别展示了感染RVA、RVB和RVC的2-3日龄仔猪的水肿、绒毛萎缩和绒毛坏死的组织病理学结果。为便于比较,图1d显示了正常绒毛的组织病理学。
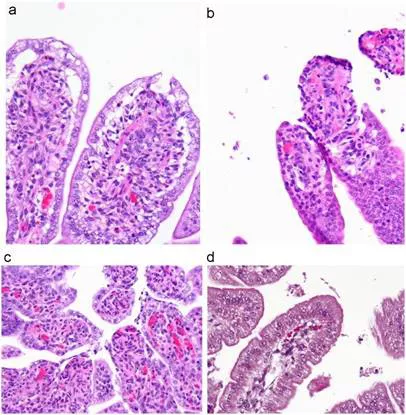
图1 RVA、RVB和RVC的组织病理学
七、诊断
诊断RV感染需要实验室确认,因为很多病原可引起猪只的腹泻,包括猪流行性腹泻病毒、传染性胃肠炎、大肠杆菌、产气荚膜梭菌等。用于检测RV感染的样本包括粪便样本、肠组织和肠内容物(Kahn&Line,2005)。鉴定方法包括电镜、聚丙烯酰胺凝胶电泳(PAGE)、病毒分离、酶联免疫吸附试验(ELISAs)、免疫组化(IHC)、RT-qPCR和下一代测序。这些测试的优点和局限性将在第2章中详细描述。
八、控制、预防和治疗
在商业猪群中根除RV几乎是不可能的,因为它无处不在。传染性RV病毒颗粒可在4℃的粪便中存活两年以上,并在环境中存活9个月以上(Chandler Bostock&Mellits,2015)。这些病毒颗粒在3到9的pH值范围内是稳定的(Chang等人,2012年),而且由于RV是一种无包膜病毒,它往往更耐消毒(Chandler Bostock&Mellits,2015年)。
在大型养猪生产系统中,由于过程中涉及所有利益相关者,预防和控制RV可能变得更加复杂。RV感染的入口包括产仔舍、哺乳舍、育肥或育成舍、运输车辆、屠宰场以及在生产过程的每个阶段与人(兽医和农场工作人员)的接触。Lacapelle等人(2017年)使用RV作为肠道分子标记物,评估大型猪生产网络中利益相关者之间传播的可能性。他们的研究结果强调运输者和屠宰场是在整个猪网络中传播RV的主要媒介和载体。
在预防和控制RV时,必须考虑猪的饲养方法。在加拿大安大略省,一项流行病学研究发现,“与在连续猪流设施中饲养的猪相比,在全进、全出方式所饲养的猪有3.4倍的可能有RVA检出”(Dewey等人,2003年)。
畜牧业和生物安全措施是预防和控制猪群体内RV感染的其他方法(Lachapelle等人,2016)。建造的养猪设施应尽量减少产仔区和哺乳区的粪便堆积,易于清洁,并且应在不同批次的猪之间对地板进行消毒(Chang等人,2012年)。在每批动物之间清洗、消毒和干燥所有运输车辆和农场工具(如靴子)也很重要,以限制RV和其他感染性病原体的传播(Lachapelle等人,2016)。农场其他考虑是限制运输车辆进入和移动,因为这些车辆可以作为媒介。
选择正确的清洁程序和消毒剂对于减少猪舍RV负荷非常重要。环境中存在的有机物(粪便)的数量会对消毒剂对抗RV病毒载量的有效性产生显著影响。在Chandler Bostock&Mellits(2015)在英国进行的一项对照研究中,对四种市售消毒剂进行了调查,以了解消毒剂在代表不同农场环境的低或高有机物存在下的有效性。Biolink生产的Bi-OO-cyst®是一种基于酚解(乙醚)的消毒剂,在高有机物存在的情况下,经嗜斑试验证明可将RV表面负荷降低4 log10以上。Evans Vanodine生产的其他两种常用消毒剂,Vanadox®(过氧乙酸)和GPC8™(戊二醛),在无有机物或存在低有机物但不存在高有机物的嗜斑试验中,能够将RV病毒载量降低4 log10以上。维康S™由杜邦公司(peroxygen Components)制造,在无有机物存在或存在低有机物的情况下,在细胞斑试验中将RV表面负荷减少4 log10以上方面具有与Bi-OO-cyst®相似的功效,但在存在高有机物的情况下失去功效。
控制猪群中RV感染的另外两种方法是进行有计划的接触,也被称为“返饲”或通过大规模接种。计划性接触发生在母猪产仔前2至5周,当从农场田间毒株感染RV的粪便或肠道内容物喂给母猪时(Robbins et al.,2014)。目的是激发母猪的免疫系统,在初乳和乳汁中为其仔猪制造母源性中和抗体(Tuanthap等人,2019年)。这种做法在没有针对RV物种的疫苗的地方或在RV感染在畜群中流行的地区很常见。
目前,美国有两种经美国农业部(USDA)许可的疫苗产品,ProSystem®Rota和ProSystem®RCE(Merck Animal Health,Madison,NJ)。这些疫苗含有两种经修饰的活RVA,分别来自血清型G4(A1)和G5(A2),单独(ProSystem®Rota)或与产气荚膜梭菌C型和四种大肠杆菌菌毛抗原K99、K88、F41和987P(ProSystem®RCE)结合使用。
妊娠母猪在分娩前5周和2周肌肉注射2毫升ProSystem®RCE(Merck Animal Health,Madison,NJ)。疫苗的目的是提高母猪抗RVA的母源中和抗体的水平,这样抗体就会在母猪体内传递初乳和牛奶。本产品的标签是“有助于预防哺乳仔猪的轮状病毒腹泻、大肠杆菌病和肠毒血症”。
ProSystem®Rota仅包含两种RVA血清型,分两次给仔猪,每次一毫升。第一剂口服给药,第二剂肌肉注射给药,在断奶前7至10天(Merck Animal Health,Madison,NJ)。这种疫苗的标签是“用于预防小猪轮状病毒腹泻”。即使有可用的RVA疫苗,RV疫情仍在猪群中发生。在猪身上开发新的RV疫苗的挑战将在第3章中详细讨论。
目前,还没有针对猪RV感染的抗病毒治疗方法(Chang等人,2012年)。抗生素在治疗轮状病毒方面作用不大;但是,它可以帮助仔猪抵御同时的其他继发感染。支持性治疗,包括葡萄糖/甘氨酸电解质溶液和含L-谷氨酰胺的口服溶液,有助于治疗新生仔猪因RV引起的脱水和体重减轻(Chang等人,2012年)。一项新的支持性治疗发现,白藜芦醇:“一种二苯乙烯和一种天然存在的植物抗毒素,由几种植物产生,用于应对伤害或防止微生物感染”,当用作30日龄仔猪的饲料添加剂时,能够减少实验感染RV的仔猪的腹泻(Cui等人,2018年)。降低死亡率的其他方法是将环境温度保持在35℃左右,以尽量减少仔猪的热量损失。此外,喂养断奶仔猪的高能量饮食也可能有助于降低发病率和死亡率(Chang等人,2012年)。
猪RV感染在大多数畜群中普遍存在;然而,除非并发其他感染,否则大多数单纯RV感染在猪中不是致命的。RV种类和毒株需要在猪身上进行监控。众所周知,人类和猪之间存在着种间传播和基因重组事件。作为一项公共卫生措施,需要进行新的诊断试验,以准确检测猪体内的所有RV物种。对商品猪群中的猪RV进行监测有助于发现RV新的G和P基因型。