2019年8月6日,中国农业科学院哈尔滨兽医研究所(中国动物卫生与流行病学中心哈尔滨分中心)的《基因缺失的减毒非洲猪瘟病毒及其作为疫苗的应用》专利申请公布。
发明人为步志高、 陈伟业、赵东明、何希君、刘任强和柳金雄,专利申请日期为2019年4月26日。
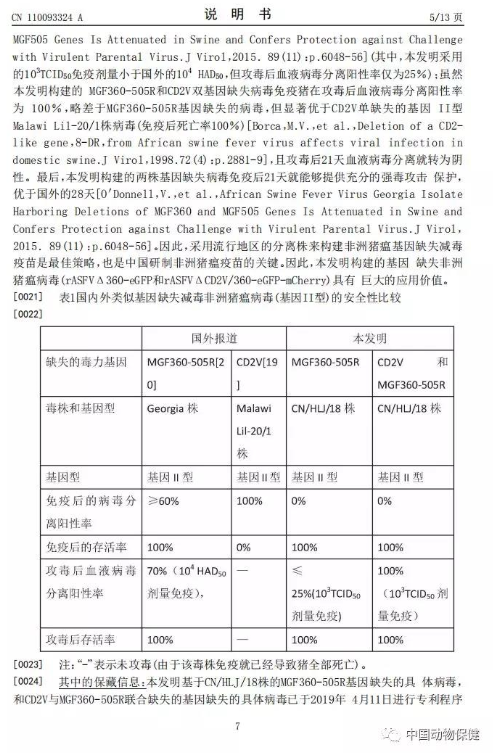
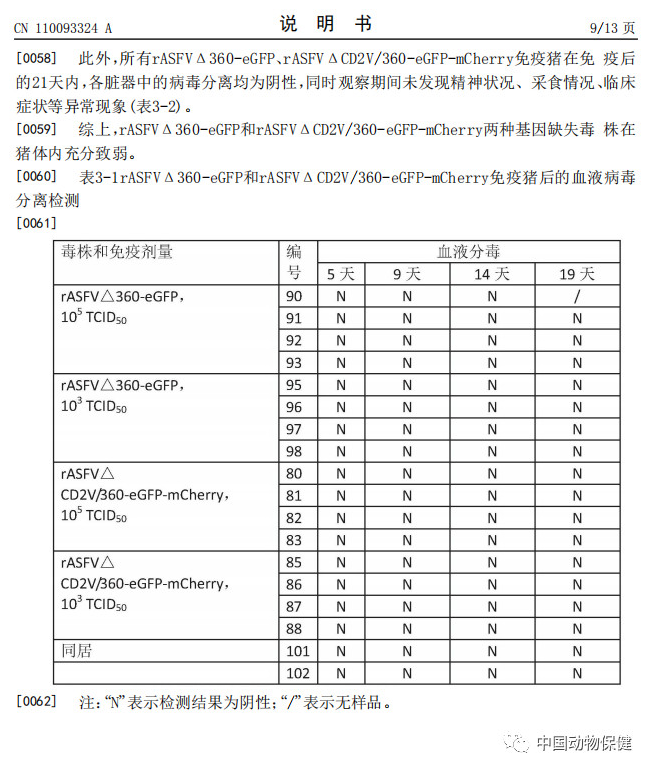
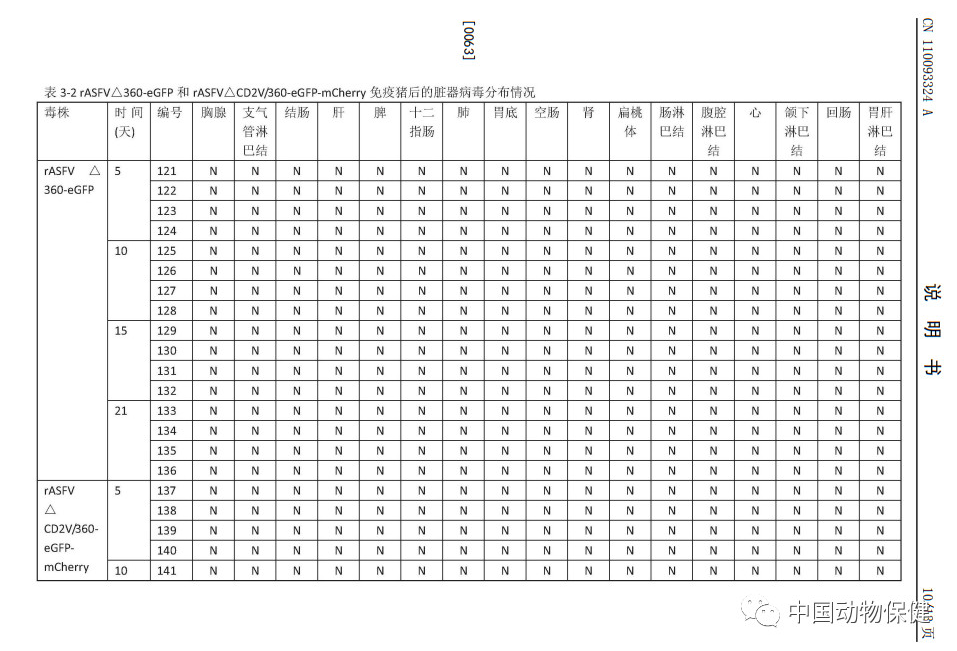
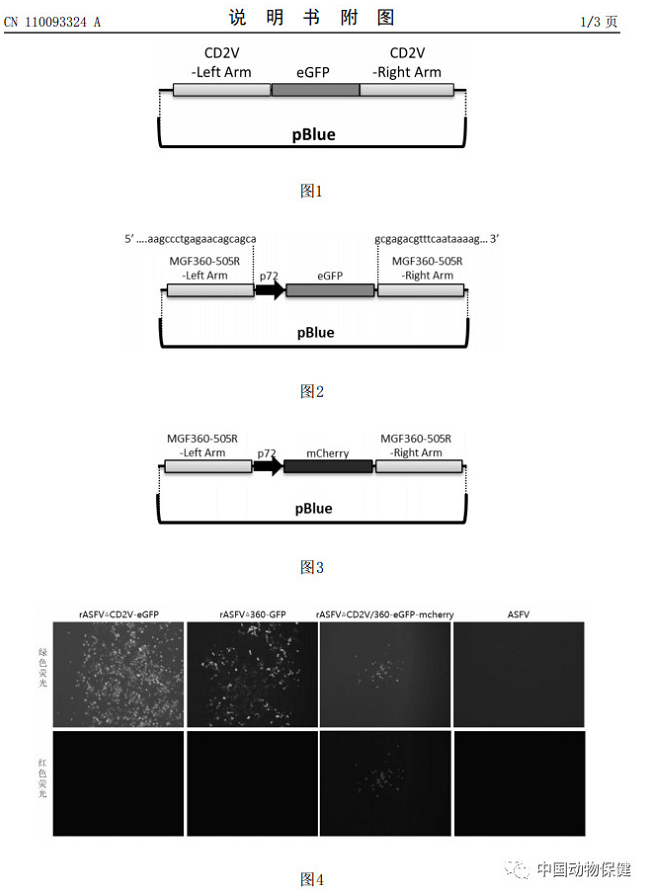
摘要显示,本发明涉及可作为疫苗的基因缺失减毒非洲猪瘟病毒及疫苗以及构建方法。本发明采用非洲猪瘟中国流行株Pig/CN/HLJ/2018,经基因工程技术,将非洲猪瘟病毒的毒力基因缺失,获得MGF360‑505R缺失和CD2V与MGF360‑505R联合缺失的基因缺失病毒。经实验表明所述两种毒株均能提供对非洲猪瘟中国流行强毒株的100%免疫保护,可作为安全和有效的防控中国非洲猪瘟疫情的疫苗,具有极大的社会价值。
详情如下:
相关实验及研究成果回顾:
中国农业科学院哈尔滨兽医研究所国家非洲猪瘟专业实验室成功分离了我国第一株ASFV,对其感染性、致病力和传播能力等生物学特性进行了较为系统的研究,并建立了动物感染模型;初步阐明了我国ASFV流行毒株的基因组特点和进化关系,为我国ASF疫情的有效防控提供了重要科学依据,为检测技术和防治疫苗研发奠定了重要基础。相关研究结果发表在新发传染病专业期刊《Emerging Microbes and Infections》。
赵东明、刘任强等人利用2018年9月3日黑龙江省佳木斯疫情发病猪样品,接种猪原代肺泡巨噬细胞,成功分离出我国第一个ASFV毒株(Pig/HLJ/18)。
中国的生猪产量约占全球总产量的50%。自2018年8月非洲猪瘟病毒(ASFV)进入中国以来,该病毒已迅速扩散至中国全境,严重威胁了中国的生猪养殖业。本研究利用原代猪肺泡巨噬细胞从ASFV暴发猪场的样本中分离到ASFV 毒株Pig/Heilongjiang/2018 (Pig/HLJ/18),并采用红细胞吸附实验(HAD)、蛋白免疫印迹、免疫荧光和电镜技术对该毒株的特性进行了研究。针对ASFV p72基因的进化分析显示,Pig/HLJ/18为基因2型。病毒在原代巨噬细胞和骨髓巨噬细胞的效价可达107.2 HAD50/ml。肌肉接种103.5–106.5 HAD50不等剂量的SPF猪可出现高热、出血等急性症状。接种猪的潜伏期为3-5天,在接种后6-9天死亡;接触猪的潜伏期则为9天,在接触后的13-14天死亡。接种猪在接种后第二天出现病毒血症,接触猪的病毒血症则出现于第9天。口腔和直肠拭子分别在在接种后2-5天和接触后6-10天可检出病毒DNA。上述结果说明Pig/HLJ/18对猪具有高度致病性和快速传播能力。ASFV危胁极大,其控制和清除工作十分必要。
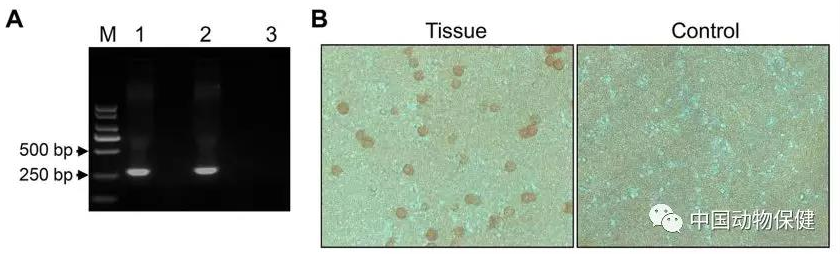
图1. 田间脾脏样本中对ASFV的检测。(A)对疑似感染猪脾脏DNA的PCR检测。第一泳道为样品,第二泳道为阳性对照质粒;第三泳道为阴性对照。(B)脾脏匀浆的红细胞吸附分析。脾脏匀浆上清被稀释10倍后接种猪PBMC细胞,添加1%猪血细胞。红细胞吸附观察期为7天。
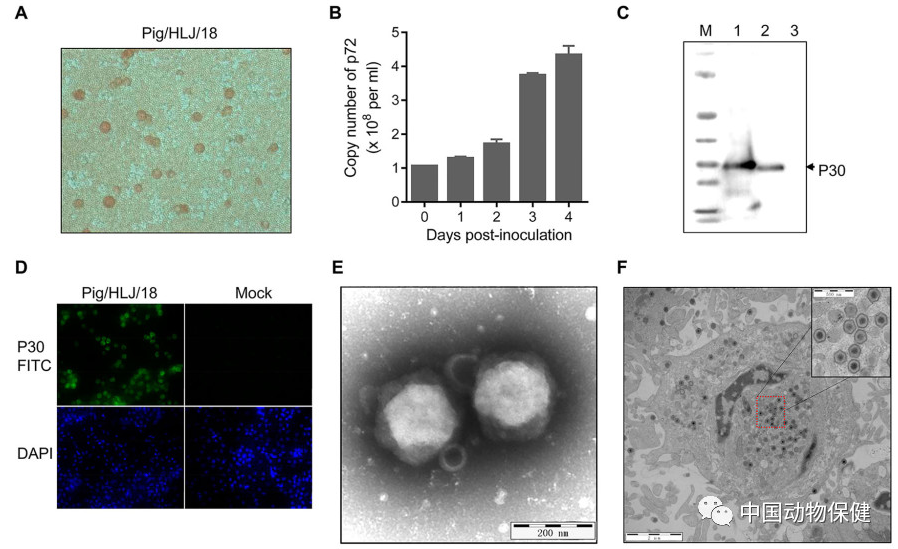
图2. 病毒在原代猪肺泡巨噬细胞上的复制。原代猪肺泡巨噬细胞接种MOI=0.2剂量的Pig/HLJ/18 ,细胞上清被用于(A)感染性病毒颗粒的检测和(B)p72基因的定量。原代猪肺泡巨噬细胞感染Pig/HLJ/18后被裂解,产物用于病毒p30蛋白的检测(C)和免疫荧光分析(D)。细胞上清中的病毒颗粒被负染后用于电镜观察(E),感染后48H的细胞被用于超薄切片观察。
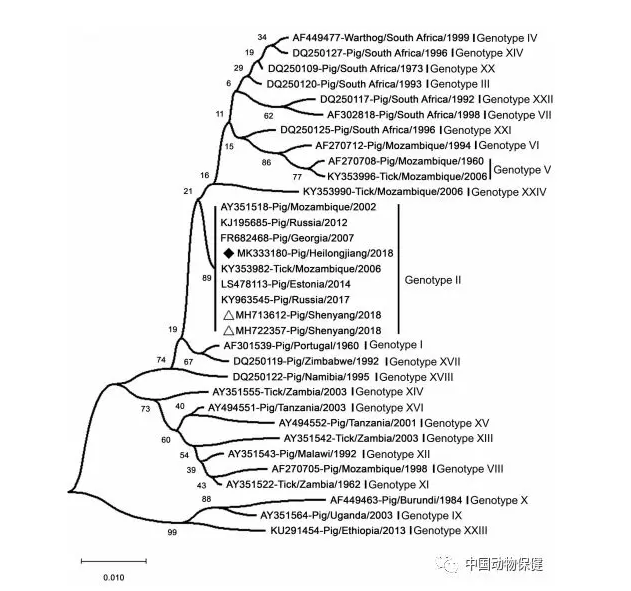
图3. 针对Pig/HLJ/18 p72基因的进化分析。ASFV参考毒株的p72基因序列下载于NCBI数据库。该图基于邻接法由MEGA X软件绘制。每个分支上的数字显示Bootstrap值>70%。本研究的ASFV分离毒为黑色菱形标记。白色三角代表中国首个案例的ASFV序列。比例尺为每个位点的核苷酸替换数。
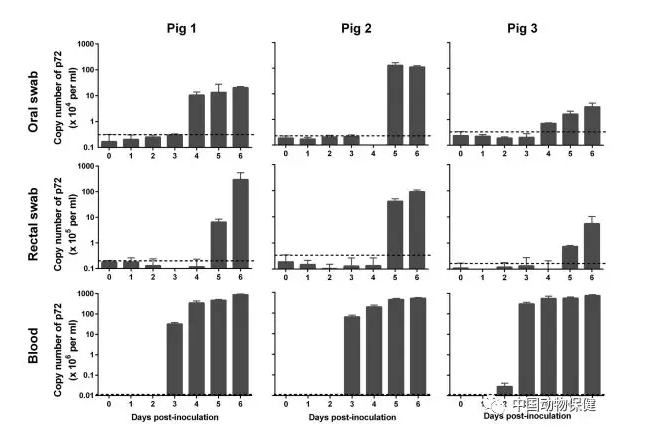
图4.Pig/HLJ/18 感染猪样本的病毒基因组拷贝数。血液、口腔拭子和直肠拭子于指定时间收集于接种剂量为103.5 HAD50 的三头感染猪。病毒p72基因的拷贝数由荧光定量方法测定。黑色虚线代表未感染组的检测极限。
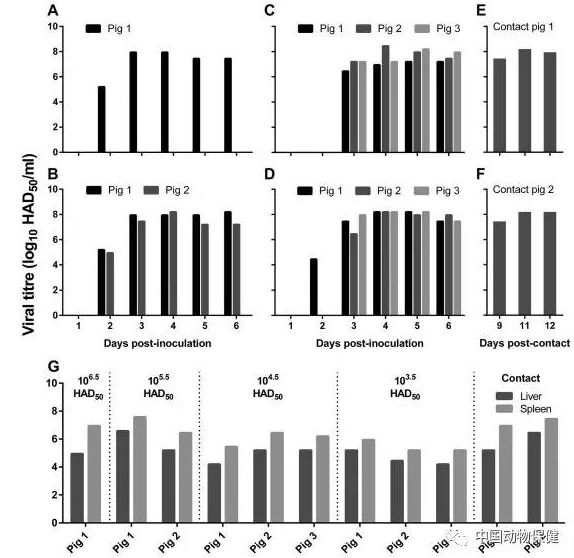
图5. HAD分析所测得的血液和器官中的病毒滴度。血液收集于不同接毒剂量的接种猪(A-D)和接触猪(E-F)。(A) 106.5 HAD50剂量接种猪; (B) 105.5HAD50剂量接种猪; (C) 104.5剂量接种猪; (D) 103.5HAD50剂量接种猪; (E)104.5HAD50剂量接种猪的接触猪; (F)03.5HAD50剂量接种猪的接触猪。(G)接种猪和接触猪肝脏和脾脏中的病毒滴度。样品收集于剖检时,每头猪的病毒接种剂量显示于每个图的上方。
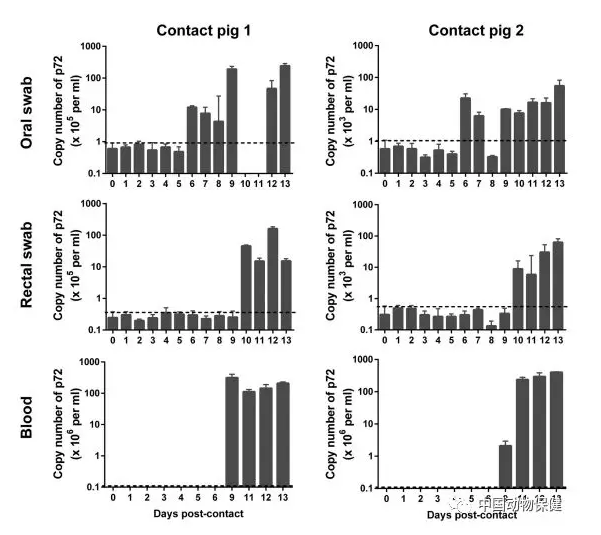
图6. 接触猪样本的病毒基因组拷贝数。血液、口腔拭子和直肠拭子于指定时间收集于两头接触猪,这两头猪分别与接种剂量为104.5 HAD50和104.5 HAD50接种猪同居。黑色虚线代表检测极限。
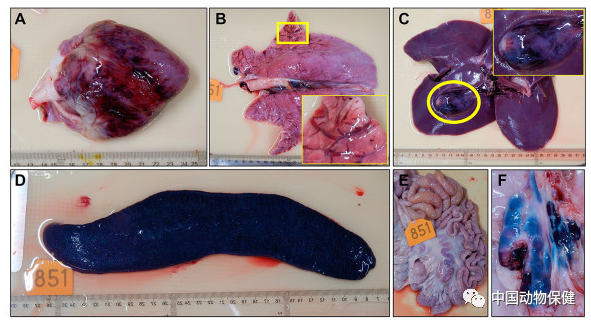
图7. 死于Pig/HLJ/18 感染的猪的脏器损伤。所有猪的损伤在附表中进行了概述。106.5HAD50接种剂量猪的心、肺、胆、脾、肠系膜淋巴结和胃肝损伤如图所示。(A)心外膜严重弥漫性出血(B)轻度肺间质水肿,插入物是对框架区域的放大(C)胆囊壁和肝脏严重出血、水肿,插入物是对圆形区域的放大(D)脾脏严重肿大、易碎、呈暗黑色(E)肠系膜淋巴结轻度肿大,外观红黑(F)胃肝淋巴结肿大出血