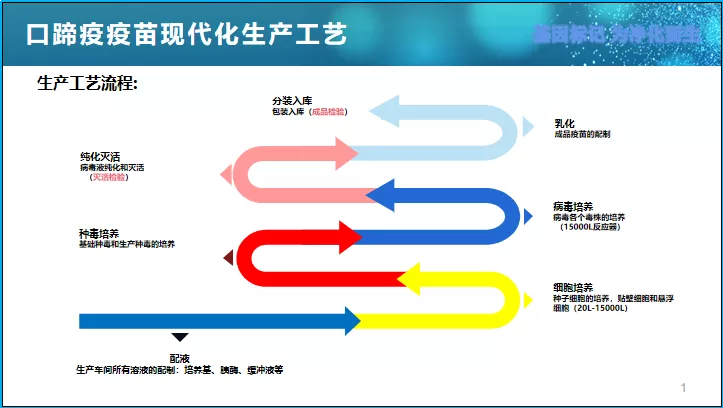
口蹄疫疫苗现代化生产工艺包括溶液配制、细胞培养、种毒培养、病毒培养、纯化灭活、乳化、分装,其中种毒、种细胞的筛选与培养、纯化灭活、乳化决定了产品的独特性与稳定性,尤其是纯化工艺代表了一个企业的生产技术水平。刘延麟博士提出,目前我国的口蹄疫疫苗生产工艺已经达到甚至超过国际先进水平,细胞培养采用悬浮培养,146S表达量大多能达到10μg/ml。
影响口蹄疫疫苗稳定性的因素
(一)口蹄疫疫苗病毒抗原
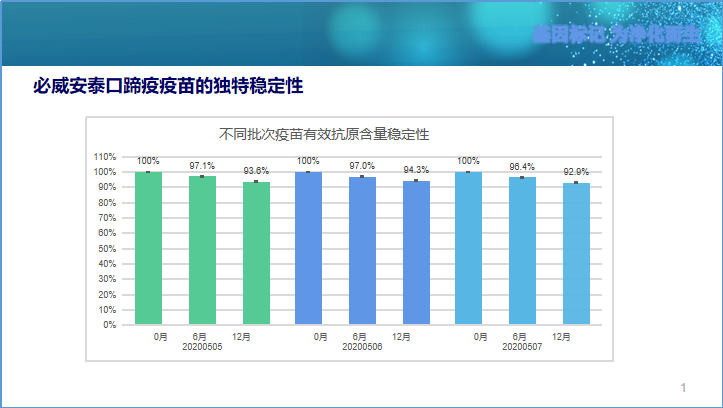
FMDV粒子的大小在25~28 nm,完整病毒粒子的沉降系数为 146S,具有最强的免疫原性。当pH低于7.0或加热条件下,FMDV会发生裂解,降解为由5个单体构成的12S前体,从而失去免疫原性。因此,如了保证病毒粒子完整不裂解,考验一个疫苗生产企业的技术力量。必威安泰采用独特的疫苗保护液配方,疫苗含量6个月内降解率在5%以内,12个月内降解率不超过10%。
(二)口蹄疫疫苗生产工艺
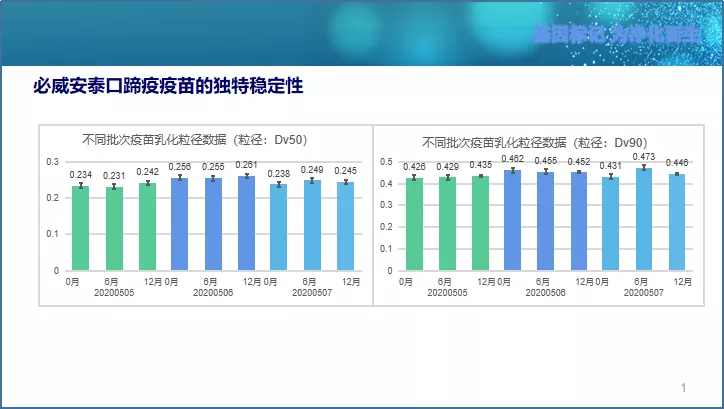
在口蹄疫灭活疫苗的生产过程中,除病毒本身生物学特性外,不同的纯化、乳化工艺不仅影响疫苗的免疫效果,同样影响疫苗的稳定性。例如抗原稀释液(缓冲体系的配方),水相(抗原)和油相(佐剂)的配比,乳化设备,乳化速度、时间、温度,佐剂等,会对疫苗的黏度、粒径大小和均匀度造成影响,是否有先进的监控或检测手段等,都会影响口蹄疫疫苗的稳定性。
(三)口蹄疫疫苗运输和储存
疫苗的保存温度为2~8℃,温度太高或冷冻均易导致疫苗有效抗原的降解或破乳。在疫苗的保存、运输、使用时未严格按照温度要求均可影响疫苗的稳定性免疫效果,如疫苗在保存和运输未使用冰块或离开冷链时间过长、使用时未做遮光处理甚至直接被日光照射、疫苗开瓶后未及时用完、在4℃和室温25℃之间反复,均导致疫苗质量降低,降低疫苗免疫效果甚至免疫失败。
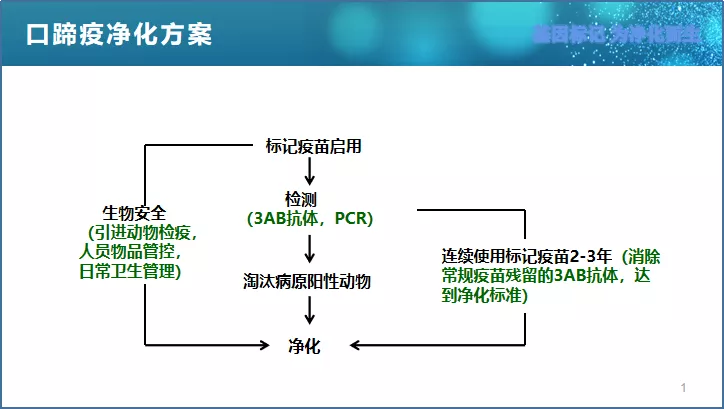
口蹄疫的净化

口蹄疫病毒由结构蛋白和非结构蛋白组成,非标记疫苗中始终有3ABC蛋白,多次免疫后3ABC抗体累积,也能检测到。根据世界卫生组织的规定,只要检出一定数量的非结构蛋白抗体,就判定不能达到免疫无疫状态。因此,使用标记疫苗免疫后,用对应的鉴别试剂盒就能判定非结构蛋白抗体到底是由野毒还是疫苗产生的。
在疫苗中添加外源抗原可作标记,但有如下问题:加什么外源抗原能满足唯一性,加多少外源抗原能满足与病毒抗原等量关系,多次免疫后难以鉴别感染。必威安泰利用反向遗传操作技术,缺失病毒的非必需基因,可作标记;与病毒抗原一起翻译,量比关系得当,能满足任何状况的感染与免疫鉴别。刘延麟博士提出,通过使用标记疫苗、检测、淘汰病原阳性动物,2~3年时间就可以达到净化标准。目前已进行部分省份无疫区建设项目,包括宁夏、四川、山东等。