
各有关单位:
为落实非洲猪瘟常态化防控,做好疫情监测排查技术支撑,按照农业农村部畜牧兽医局要求,我中心将于近期组织开展非洲猪瘟病毒抗体检测试剂盒评价。现将有关事项通知如下。
一、评价原则
评价工作遵循公开、公正、科学、实用的原则。
二、评价范围
参评产品为非洲猪瘟病毒抗体检测ELISA试剂盒中试产品(ELISA试剂盒所用方法应符合《非洲猪瘟诊断技术GBT18648-2020》规定的抗体检测要求)。
三、送评单位
已取得中华人民共和国兽药GMP证书的国内生产企业,且兽药GMP证书验收范围包含免疫学类诊断制品生产线。
同一企业送评产品不超过两个。同一企业送评的不同产品应为不同ELISA方法(间接ELISA、阻断ELISA或夹心ELISA等)。同一产品只能由一家生产企业送评。
四、评价内容
参评试剂盒的分析特异性、分析敏感性、诊断特异性、诊断敏感性、重复性等特性。
五、有关要求
(一)各送评单位于2021年4月26日前,将非洲猪瘟病毒抗体检测试剂盒送评登记表(附件1)纸质版、文审材料(具体要求见附件2)纸质版和试剂盒(具体要求见附件3)送至中国动物疫病预防控制中心大兴基地;登记表和文审材料电子版发送至cadcasfv@163.com。
(二)各送评单位应对送评产品的真实性、合法性负责。严禁伪造试剂盒和文审材料,一经发现,立即取消参评资格。
六、联系方式
中国动物疫病预防控制中心 兽医诊断室
联系人:刘颖昳、胡迪
联系电话:59198949/59198950
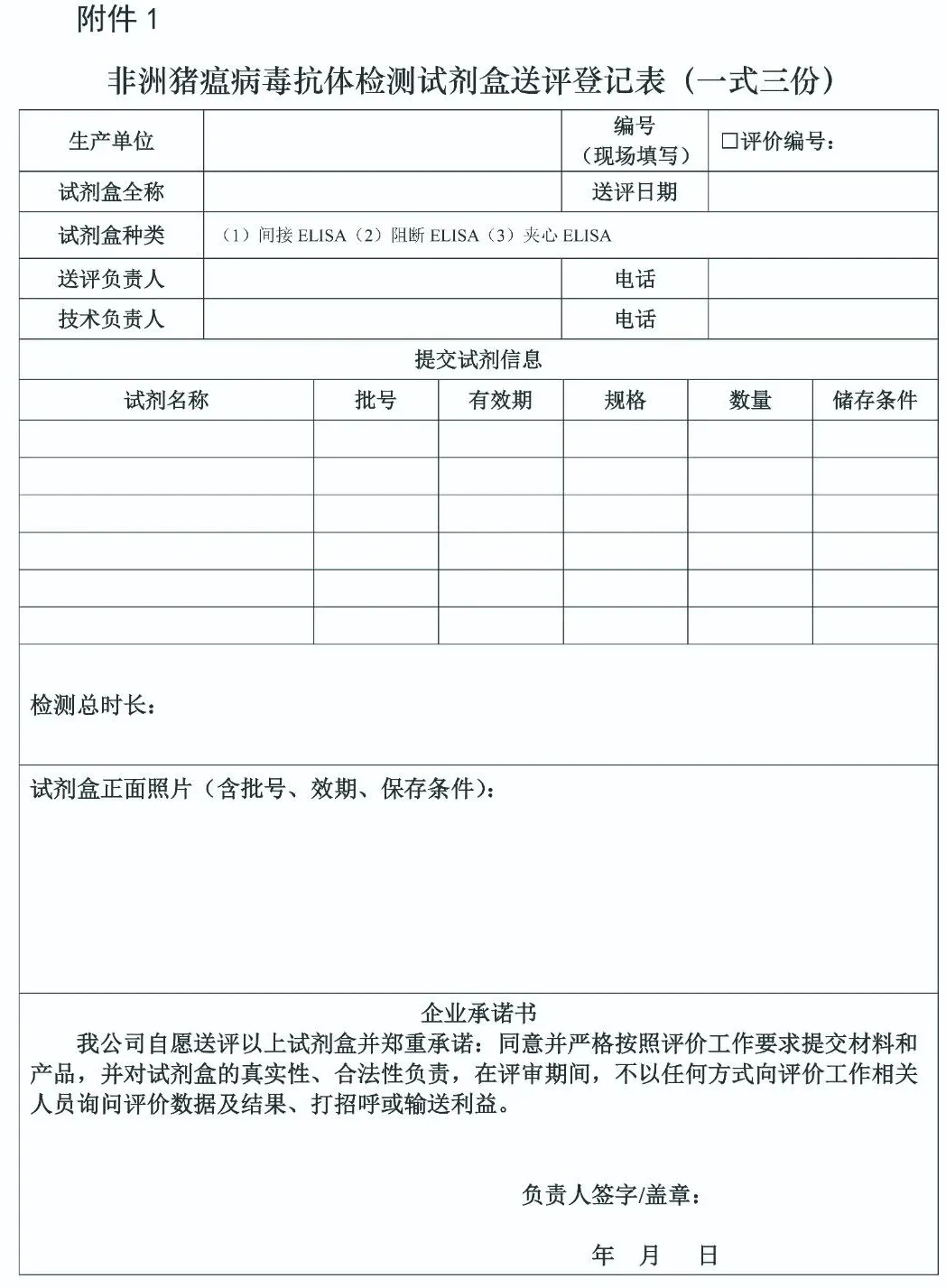
附件2
非洲猪瘟病毒抗体检测试剂盒评价文字材料清单
一、材料内容
1. 单位法人证书复印件/公司营业执照复印件(与兽用GMP 证书企业名称一致);
2. 兽药GMP 证书:参评试剂盒企业的兽药GMP证书验收范围需包含免疫学类诊断制品生产线;
3. 产品质量研究报告,应包括:
(1)一般资料:诊断制品的名称;制造及检验试行规程(草案)、质量标准及其起草说明,附各项主要检验的标准操作程序。
(2)生产用菌(毒、虫)种的研究资料:来源和特性;种子批。
(3)生产用细胞的研究资料:来源和特性;细胞库。
(4)主要原辅材料的来源、检验方法和标准、检验报告等。
(5)生产工艺研究资料:主要制造用材料、组分、配方、工艺流程等资料;诊断制品生产工艺的研究资料。
(6)对照品(血清等)的制备、检验等研究资料。
(7)制品的质量研究资料:成品检验方法的研究和验证资料;诊断方法的建立和最适条件确定的研究资料;用于实验室试验的制品生产和检验报告;敏感性研究报告;特异性研究报告;至少3批诊断制品的批间和批内可重复性试验报告;至少3批诊断制品的保存期试验报告;符合率(与其他诊断方法的比较)试验报告。
(8)中间试制前的研究工作总结报告。
(9)中间试制报告。
(10)有资质实验室的测试验证报告。
4. 送评试剂的说明书、标签和包装设计样稿,可随附针对此次评价试剂盒的讲解视频。
5. 知识产权保证书。
二、提交要求
1.所有文件按序号编辑目录并装订,提交3本,封面标明试剂盒名称、试剂盒种类(间接ELISA、阻断ELISA或夹心ELISA)及生产厂家。
2.电子材料整理为一个PDF文件,以试剂盒名称+单位名称方式命名,发送至cadcasfv@163.com。
附件3
非洲猪瘟病毒抗体检测试剂盒评价送评试剂盒要求
一、送评试剂要求
每种试剂盒均需提供3个批次的试剂盒,其中的1个批次提供5个以上检测试剂盒(不少于500检测头份),另2个批次各提供2个以上检测试剂盒(每批次不少于200检测头份)。
实验室评测后,试剂盒留样封存,不予退回。
二、提交要求
所有试剂盒按批次整理包装好,外贴标签注明试剂批次,并按照保存温度要求(室温试剂、4℃试剂、-20℃试剂)分别放置。
最新发布